2021-08-05
新生儿缺氧缺血性脑病(HIE)是围产期窒息导致脑的缺氧缺血性损害且难治愈的中枢神经系统疾病,是新生儿期死亡和新生儿期后严重神经功能损害的主要原因。然而,目前针对HIE还没有令人满意的治疗方法。

近日,重庆医科大学附属儿童院儿科研究所认知发育与学习记忆障碍转化医学重庆市重点实验室董志芳教授团队在国际学术期刊《Cell Death and Differentiation》(2021 IF:15.828)上发表题为“Aagab acts as a novel regulator of NEDD4-1-mediated Pten nuclear translocation to promote neurological recovery following hypoxic-ischemic brain damage”的文章,报道发现Aagab作为NEDD4-1新的调控因子可以调控NEDD4-1介导的PTEN核转移,基于此合成的Tat-K13多肽可以抑制PTEN核转移,缓解HIBD引起的神经损伤,改善运动和神经认知功能。

作者发现在模拟新生儿HIE的新生鼠缺氧缺血性脑损伤(HIBD)模型中缺氧缺血后总蛋白中PTEN蛋白水平没有变化,但是细胞核内蛋白水平呈时间依赖性增加。作者进一步采用原代培养神经元予氧糖剥夺(OGD)模拟在体缺氧缺血,发现OGD后PTEN核转移呈时间依赖性增加。
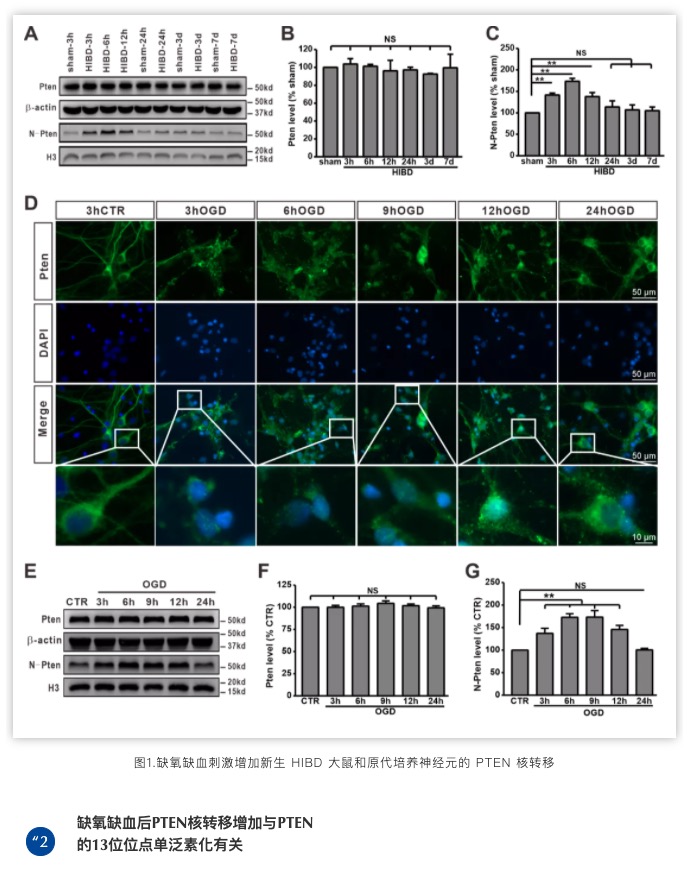
OGD引起PTEN单泛素化增加,PTEN核转移增加,予PTEN13位位点突变后减少OGD引起的PTEN单泛素化,进而减少OGD引起的PTEN核转移。
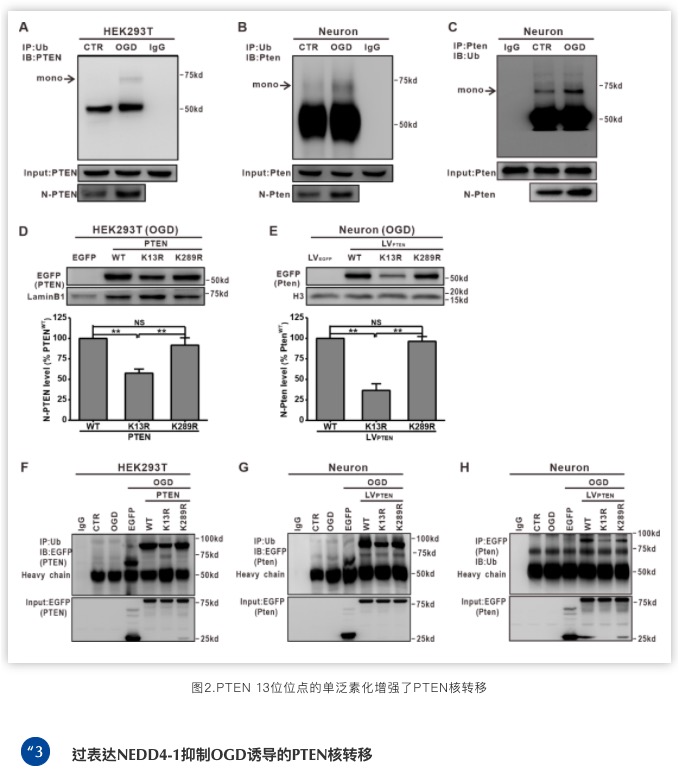
为了寻找缺氧缺血诱导PTEN核转移的分子机制,课题组通过慢病毒干扰和过表达既往有文献报道的PTEN的E3泛素连接酶NEDD4-1和NEDD4-1,发现调控NEDD4-2蛋白水平对PTEN核转移没有影响,而OGD前过表达NEDD4-1能抑制OGD诱导的PTEN核转移。
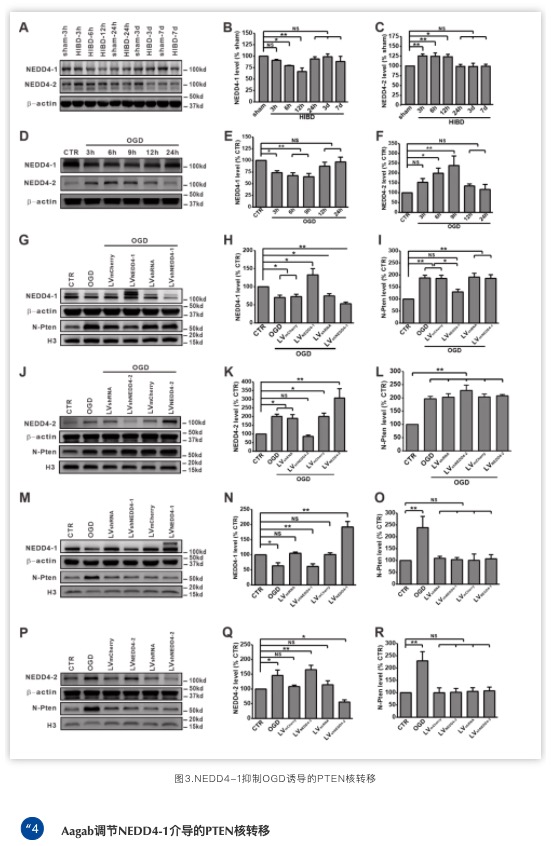
为了进一步探索NEDD4-1在OGD介导的PTEN核转移中的机制,我们找到参与蛋白膜转运具有Rab样GTP酶结构域蛋白Aagab,发现Aagab可以通过调控NEDD4-1蛋白水平调控PTEN核转移,下调Aagab蛋白水平后NEDD4-1蛋白水平降低,PTEN核转移增加,而过表达NEDD4-1能部分抑制Aagab下调引起的PTEN核转移。
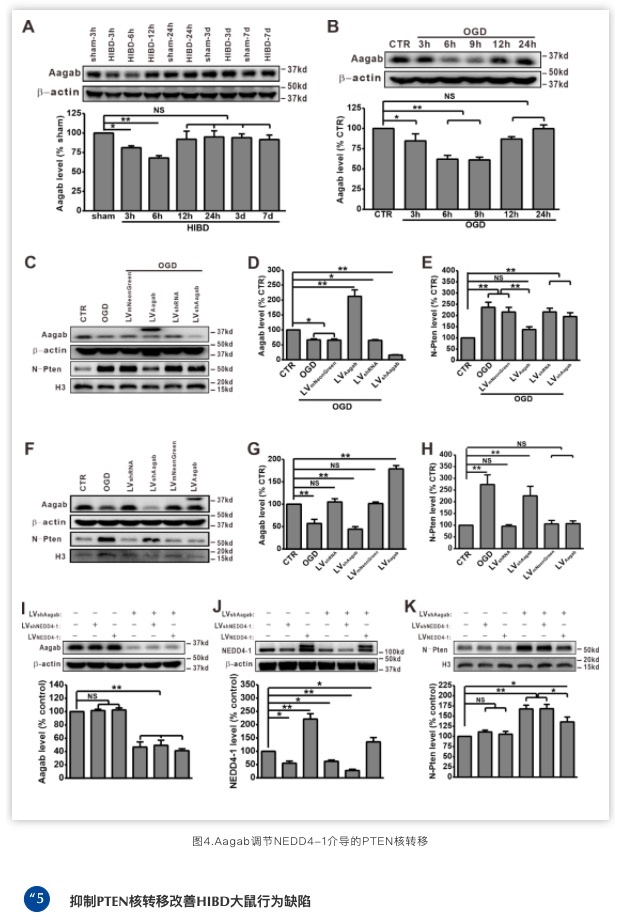 、
、
基于PTEN的K13单泛素化在核转移中的重要作用,合成了抑制PTEN入核的多肽Tat-K13(一种基于PTEN K13残基的干扰短肽),在HIBD模型大鼠上,发现Tat-K13不仅能抑制PTEN核转移,而且可以逆转HIBD后运动和认知功能损伤。
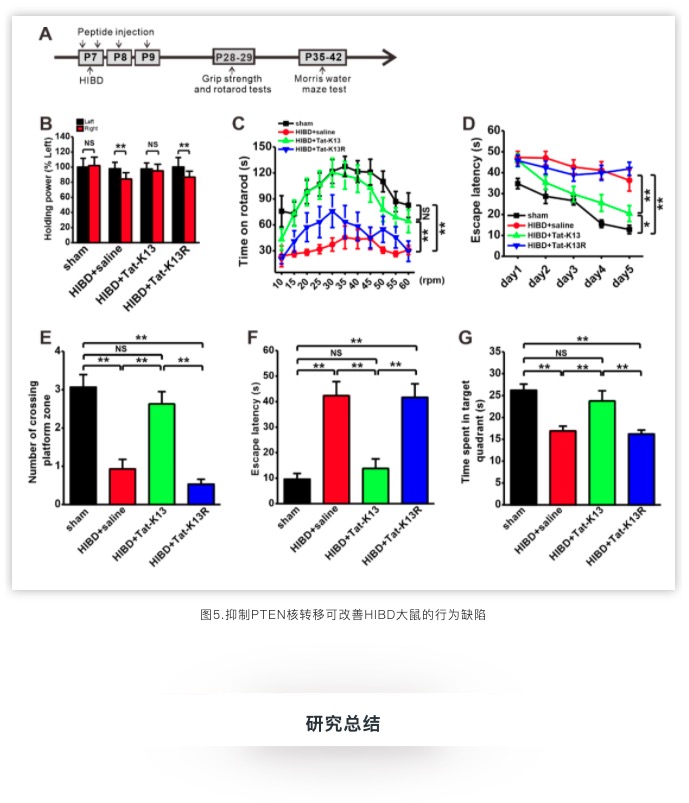
课题组首先建立HIE动物模型—新生鼠缺氧缺血性脑损伤(HIBD)模型,发现HIBD后PTEN转移入核明显增加。通过对原代培养神经元进行氧糖剥夺(OGD)处理,模拟体内缺氧缺血,发现OGD诱导的PTEN核转移增加与PTEN的13位赖氨酸残基(K13)单泛素化有关。通过点突变将PTEN的13位赖氨酸残基(K)突变成精氨酸(R),可以抑制OGD诱导的PTEN核转移,对神经元损伤起到保护作用。通过慢病毒干扰和过表达NEDD4-1,发现OGD前过表达NEDD4-1能抑制OGD诱导的PTEN核转移。进一步深入研究发现Aagab可以通过调控NEDD4-1蛋白水平调控PTEN核转移。基于PTEN的K13单泛素化在核转移中的重要作用,合成抑制PTEN入核的多肽Tat-K13,发现Tat-K13不仅能抑制PTEN核转移,而且可以逆转HIBD后运动和认知功能损伤。
文章首次报道Aagab作为新的调控因子可以调控NEDD4-1介导的PTEN核转移,基于此合成的Tat-K13多肽可以抑制PTEN核移,缓解HIBD引起的神经损伤,改善运动和神经认知功能,为临床治疗新生儿缺氧缺血性脑病提供了新的靶点和干预措施。

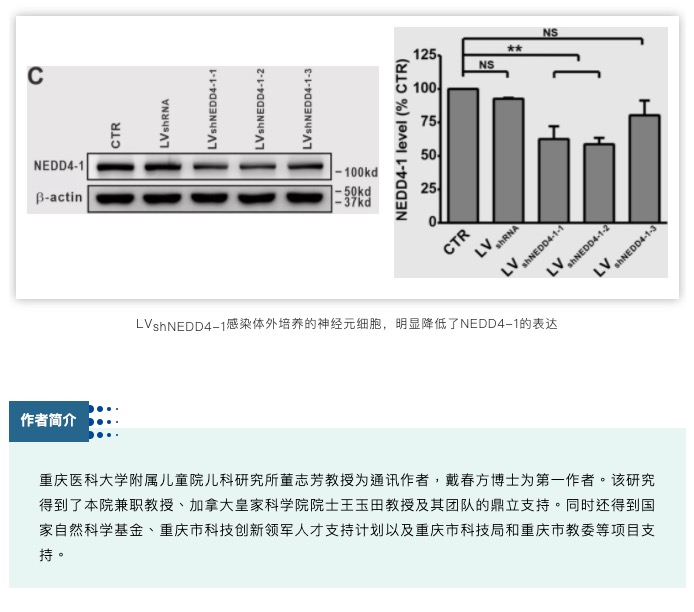
NEDD4-1干扰慢病毒LVshNEDD4-1 由吉凯基因提供,用于感染神经元细胞。
LVshNEDD4-1-1:5’-AGCCACAAATCAAGAGTTAAA-3’
LVshNEDD4-1-2:5’- TTGGAAGGACCTACTACGTAA -3’
LVshNEDD4-1-3:5’- CTGGATTGAGTTTGATGGTGA -3’
预实验结果证明LVshNEDD4-1-1的敲减效果最好。
© 2023 GENECHEM All RIGHTS RESERVED .
© 2023 GENECHEM All RIGHTS RESERVED .
